
tabla de números de oxidación
En la tabla tienes los números de oxidación más habituales de los elementos. Están relacionados con su situación en la tabla periódica y con las característias de los enlaces que forman, como ya viste en la unidades 1 y 2: por ejemplo, en los alcalinotérreos -grupo 2- es +2 porque como tienen dos electrones en la capa más externa tienen tendencia a perderlos para alcanzar la.

Números de Oxidación MÁS QUE APUNTES
a) Los números de oxidación apropiados son. Los únicos átomos que cambian son Mn, de +7 a +2, una reducción, y S, de +4 a +6, una oxidación. La reacción es un proceso redox. SO 2 ha sido oxidado por MnO 4 —, y entonces MnO 4 — es el agente oxidante. MnO 4 — se ha reducido en SO 2, y así SO 2 es el agente reductor.

Nomenclatura de los Compuestos Tabla números de oxidación
La tabla periódica es una herramienta práctica para comprender la química. Está diseñada para mostrarnos la estructura de los elementos y cómo se relacionan entre sí. Los números de oxidación son una parte importante de la tabla periódica que nos ayuda a entender cómo los elementos se relacionan con los demás.

numero de oxidacion de los elementos de la tabla periodica Brainly.lat
Los números de oxidación son una herramienta fundamental en la química que nos permite determinar el grado de carga de los átomos en un compuesto. Estos números representan la cantidad de electrones que un átomo ha ganado o perdido en una reacción química. Conocer los números de oxidación es esencial para comprender y predecir el.

Numero de oxidacion de todos los elementos de la tabla periodica Brainly.lat
Los halógenos (grupo 17, o grupo del F) tienen 7 electrones de valencia, tenderán a ganar 1 poseyendo siempre con el H y con los metales número de oxidación -1. Dentro de los metales de transición debemos saber que la Ag tiene número de oxidación +1 , el Zn y Cd tienen número de oxidación +2, y el Sc, Y y La tienen número de.
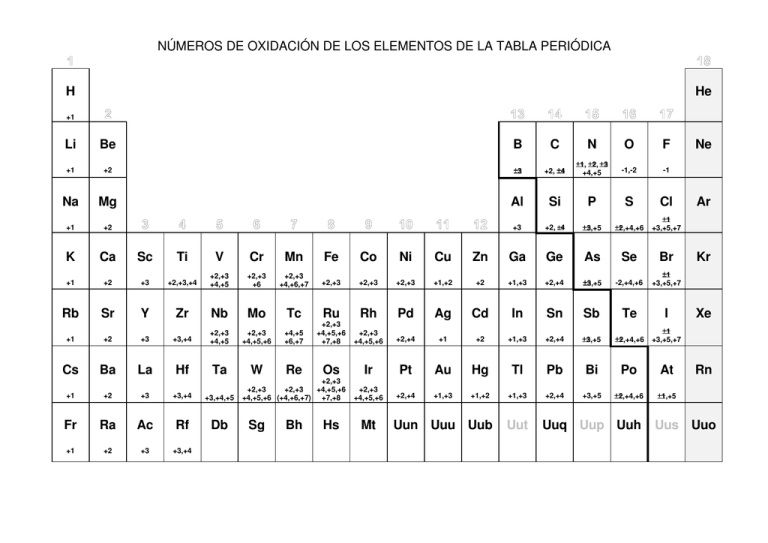
NÚMEROS DE OXIDACIÓN DE LOS ELEMENTOS DE LA TABLA
Si identificamos al anión carbonato, CO32-, el cálculo de todos los números de oxidación será sencillo. Empezamos por el mismo carbonato, sabiendo que el número de oxidación del oxígeno es -2: Puede servirte: Operaciones unitarias. (CxO32-)2-. La sumatoria de los números de oxidación debe ser igual a -2: x + 3 (-2) = -2.

FÍSICA Y QUÍMICA "IES EUGENIO HERMOSO" Números de Oxidación
Por ejemplo, el hierro común tiene un número de oxidación de +2 o +3. Los halógenos, por otro lado, tienen un estado de oxidación de -1. Esta tabla periódica contiene los números de oxidación de los elementos, así como los números, símbolos, nombres y pesos atómicos de los elementos.
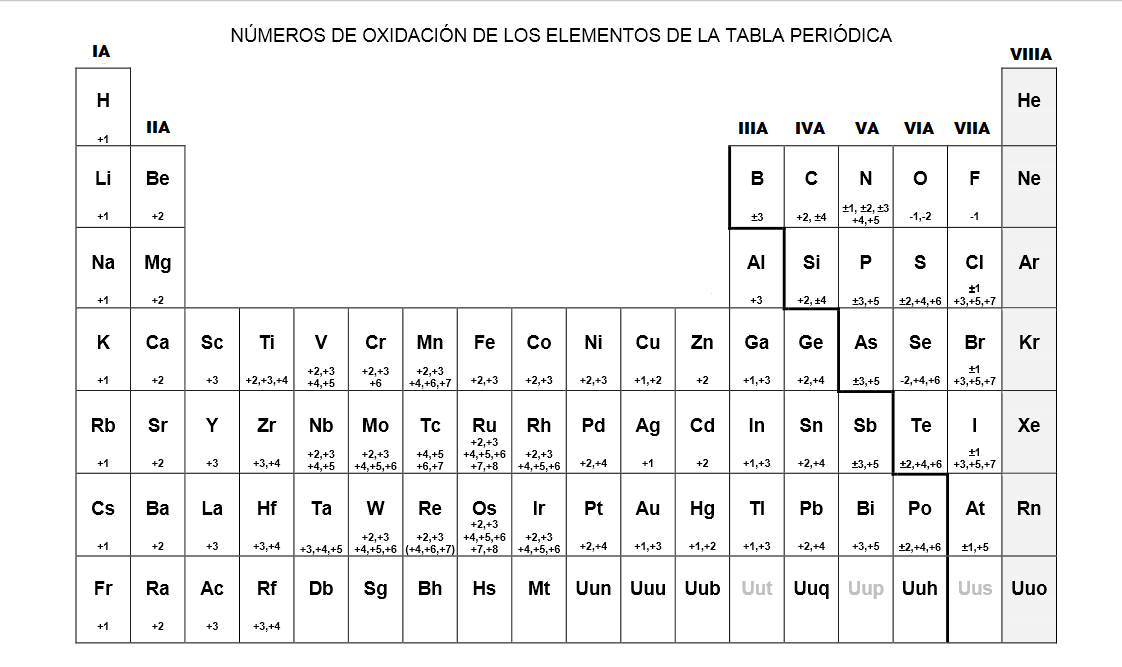
Nomenclatura de los Compuestos Tabla números de oxidación
La Tabla Periódica de Números de Oxidación es una herramienta útil para comprender la forma en que los elementos químicos interactúan entre sí. Esta tabla contiene información sobre la forma en que los elementos químicos cambian su estado de oxidación al combinarse con otros elementos. Esta tabla se utiliza ampliamente para comprender.

Números de Oxidación de los Elementos de la Tabla Periódica. Fácil y rápido de entender. Además
CALCULADORA DE NÚMEROS DE OXIDACION. Para calcular de los números de oxidación de los elementos de un compuesto químicos, escribre su fórmula y dale clic en 'Calcular' (por ejemplo: Ca2+, HF2^-, Fe4 [Fe (CN)6]3, NH4NO3, so42-, ch3cooh, cuso4*5h2o ). The oxidation state of an atom is the charge of this atom after ionic approximation of its.

QUÍMICA blog de Carlos numeros de oxidacion
El número de oxidación de un elemento en su estado libre es cero, 0. Por ejemplo: H 2, O 2, P 4, etc. = 0. El número de oxidación de iónes monoatómicos es igual a la carga de dichos iones. Por ejemplo: Na + = +1, Ca 2+ = +2; Cl - = -1. El número de oxidación del hidrógeno es +1 en todos sus compuestos, excepto en los hidruros.
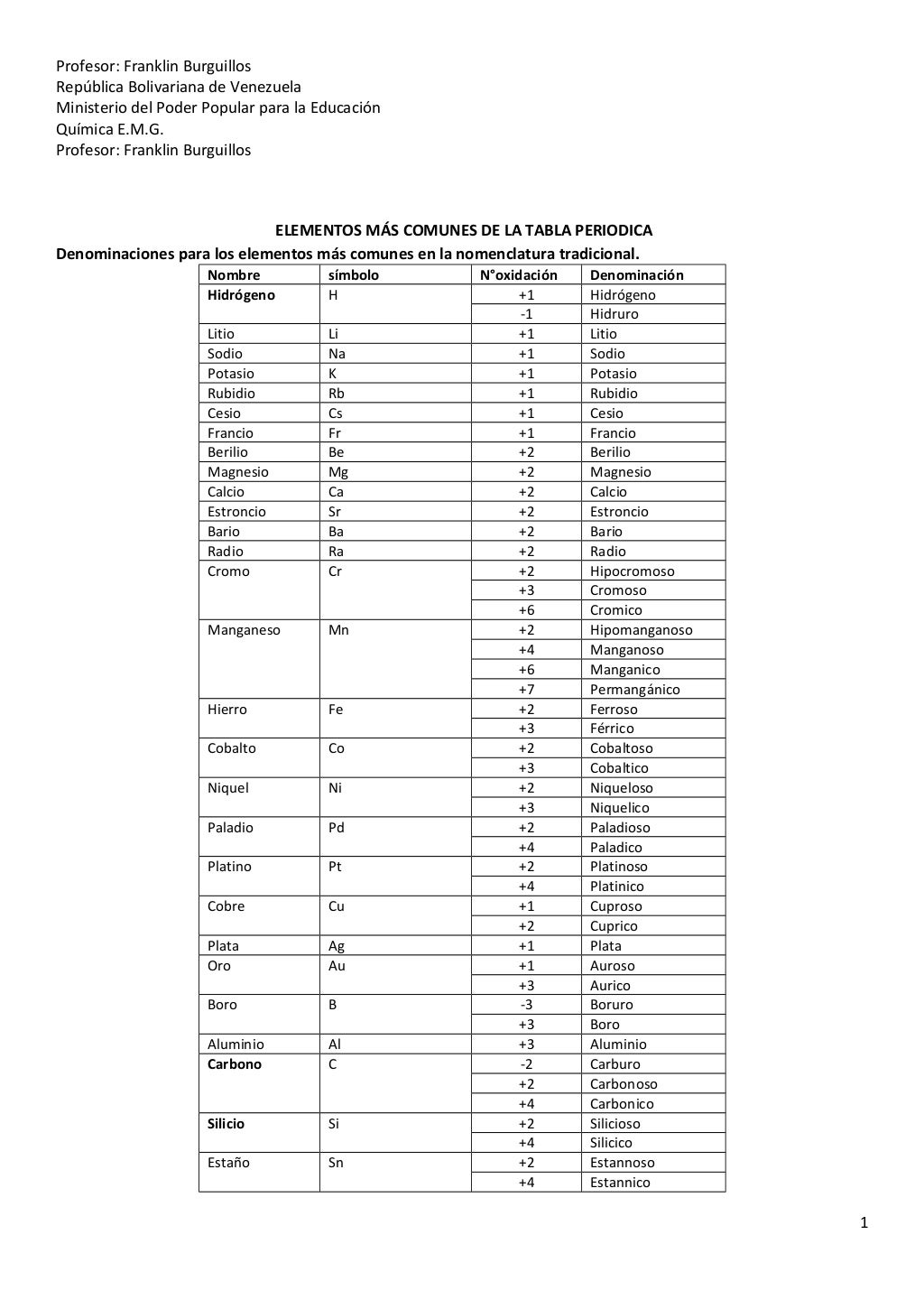
Tabla periódica con los número de oxidación de los elementos más comu…
Anexo. : Estados de oxidación de los elementos. Esa es una lista de los elementos químicos, excluyendo aquellos valores no enteros. Los estados más comunes aparecen en negrita. La tabla está basada en una realizada por Greenwood and Earnhshaw con notas añadidas. El estado de oxidación 0, que ocurre para todos los elementos, viene.
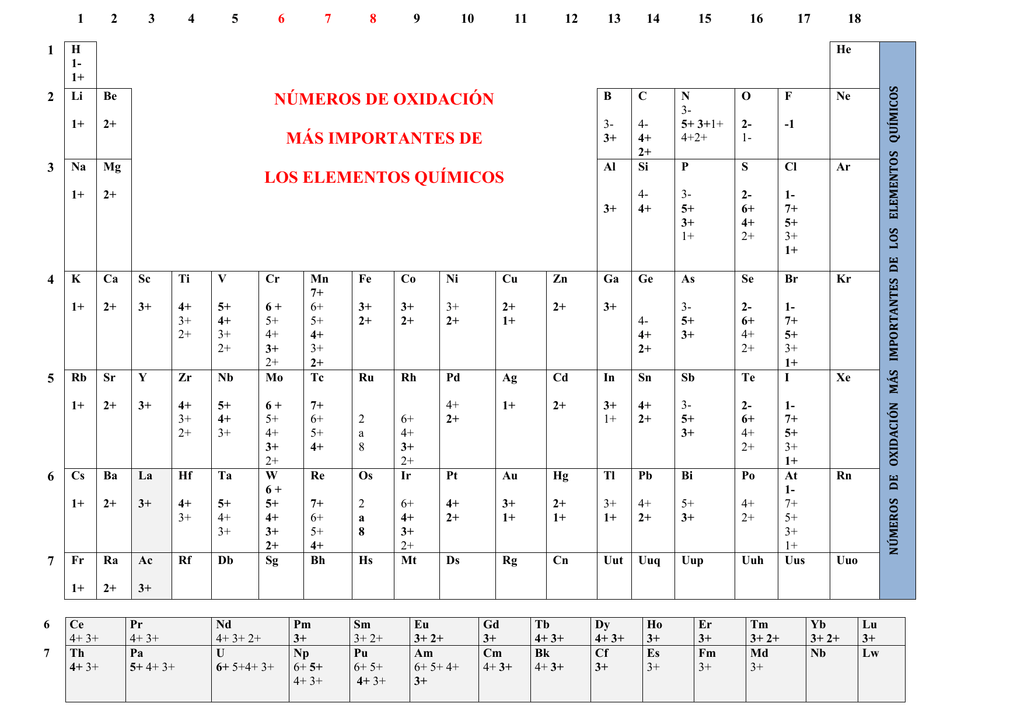
números de oxidación más importantes de los elementos químicos
Para los demás elementos principales de la tabla periódica, que poseen más de un número de oxidación, nos guiaremos por la clasificación descrita en la siguiente tabla. Números de oxidación de los principales elementos de la tabla periódica. Elementos Números de oxidación Grupo 1 o IA Li, Na, K, Rb, Cs, Fr +1 Grupo 2 o IIA

QUIMICAGIMNASIANO TABLA CON NÚMEROS DE OXIDACIÓN GRADO OCTAVO (IMPRIMIR)
Tabla de números de oxidación (valencias): Anuncio. Tabla de números de oxidación (valencias): NO METALES H ( hidrógeno) F (flúor) Cl (cloro) Br (bromo) I (yodo) O (oxígeno) S (azufre) Se (selenio) Te (teluro) N (nitrógeno) P (fósforo) As (arsénico Sb (antimonio) Bi (bismuto) B (boro) C (carbono) Si (silicio) METALES 1 -1 1, 3, 5, 7 2.
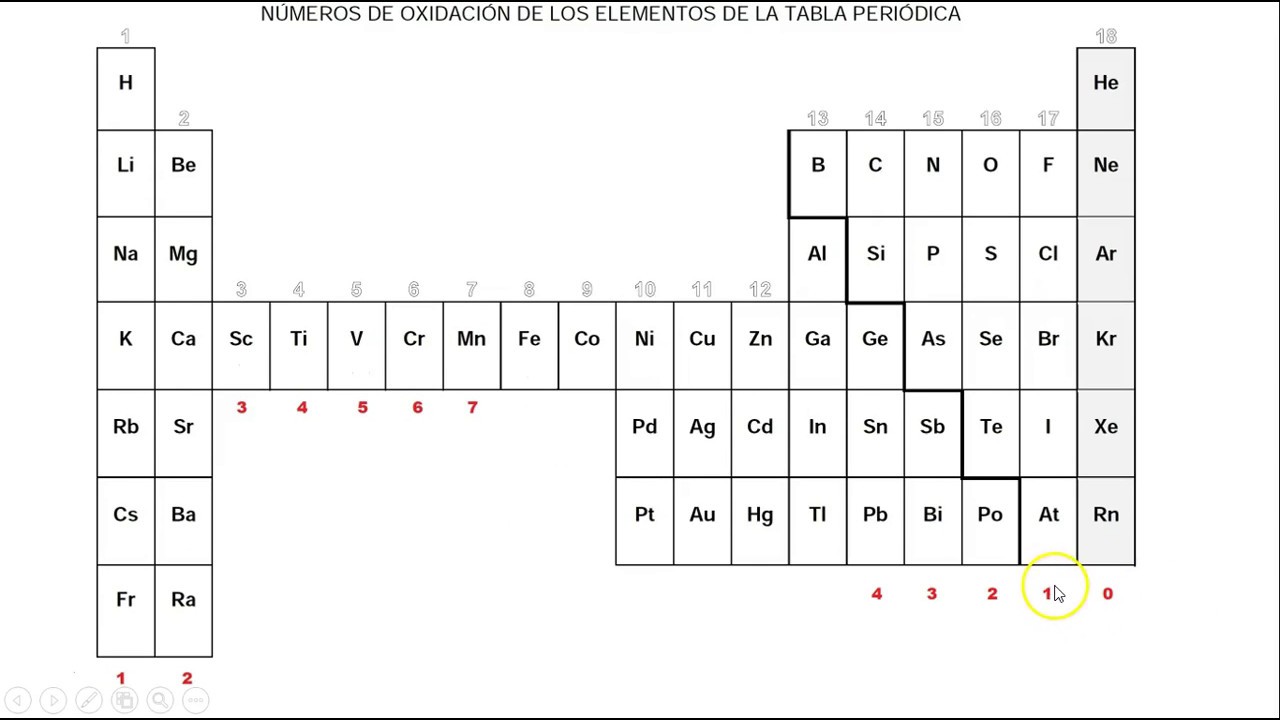
APRENDER LOS NÚMEROS DE OXIDACIÓN FÁCILMENTE YouTube
Ejemplos de números de oxidación. Veamos ejemplos específicos de números de oxidación en diferentes compuestos. 1. Ácido clorhídrico (HCl): el número de oxidación del cloro es -1. 2. Sulfato de sodio (Na2SO4): el número de oxidación del azufre es +6. 3. Óxido de hierro (Fe2O3): el número de oxidación del hierro es +3.

Numero oxidacion de la tabla periodica.
1.El Número de Oxidación de todos los Elementos en Estado Libre, no combinados con otros, es cero (p. ej., Na, Cu, Mg, H2, O2, Cl2, N2). 2. El Número de Oxidación del Hidrógeno (H) es de +1, excepto en los hidruros metálicos (compuestos formados por H y algún metal), en los que es de -1 (p. ej., NaH, CaH2).
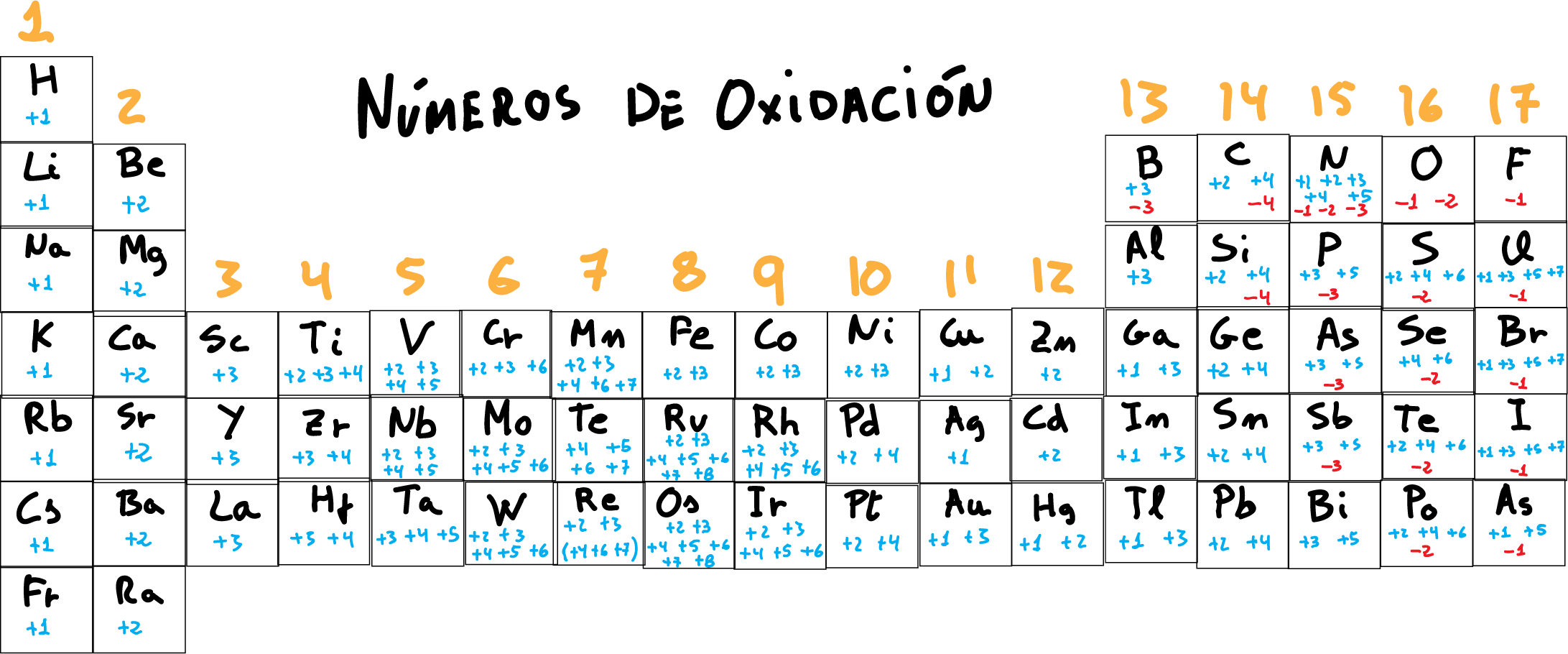
Número de Oxidación Definición, Cálculo De Química
22.6: Asignación de Números de Oxidación. Pasando de estudiar el elemento hierro a compuestos de hierro, necesitamos poder designar claramente la forma del ion hierro. Un ejemplo de esto es el hierro que se ha oxidado para formar óxido de hierro durante el proceso de oxidación.